在20世纪90年代,研究者们在海外揭开了BRCA1与BRCA2基因与遗传性乳腺癌的关联,这一成果具有划时代的意义。著名影星安吉丽娜·朱莉由于BRCA1基因突变,其乳腺癌发病几率高达87%,于是她决定切除乳腺和卵巢,这一举措引发了公众的极大关注。同时,人们开始研究通过移除胚胎中的BRCA1基因来减少癌症风险的可行性,这一议题成为了研究的新焦点。
BRCA基因与患癌风险
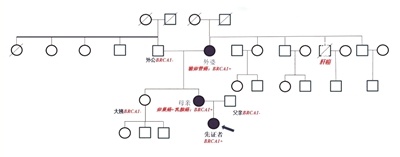
20世纪90年代,研究者们揭露了BRCA1和BRCA2基因与乳腺癌遗传性之间的关联。这一突破性发现,对肿瘤遗传学领域产生了深远影响。这些基因变异的携带者,其癌症风险远超常人。以安吉丽娜·朱莉为例,她因BRCA1基因变异,乳腺癌发病概率高达87%。这一情况促使人们深入探索基因与癌症的内在联系。
研究数据显示,基因在癌症形成过程中扮演着关键角色。在医学研究领域,这些高风险基因的发现为癌症的预防及治疗方法的研究提供了明确的方向。
生殖辅助技术的应用现状
黄荷凤院士强调,第三代试管婴儿技术拥有阻断遗传致病基因的功能。以杜氏肌营养不良和血友病等单基因遗传病为例,浙江大学附属妇产科医院自90年代初便开展了相关研究。此技术为众多面临遗传病风险的家庭带来了新的希望,可在胚胎早期阶段对有害基因进行筛选。
乳腺癌等疾病,因涉及多个基因,具有家族聚集性和遗传易感性等特点,其复杂性有所增加。尽管在单基因遗传病的治疗上,技术已取得显著进展,但在多基因疾病的治疗上,相关经验却相对不足,两者形成了显著的反差。
多基因遗传癌症的风险挑战
乳腺癌的发生部分与基因突变相关,其中BRCA1和BRCA2基因的变异是原因之一,然而在家族性乳腺癌病例中,此类基因变异所占比例较小。除了这两种基因外,还存在许多其他遗传变异位点,它们与乳腺癌的易感性相关。即便运用第三代试管婴儿技术移除BRCA1基因,也无法彻底消除由多基因遗传引起的癌症风险,这成为了当前面临的重要挑战。
在癌症预防和控制的领域,单纯针对单个基因的干预手段已被证明是不够的。这一发现表明,癌症的多基因遗传风险背后,隐藏着一种更为复杂的遗传作用体系。
新思路的提出
黄荷凤院士研发了一项新技术。该技术能够对胚胎的多基因疾病遗传风险进行评估,具体做法是通过多基因遗传风险评分。基于此评估,团队筛选出风险最低的胚胎用于移植,从而实现对多基因遗传病的一级预防。经过家系验证和生殖伦理的审查,该团队以莺歌案例为试点,开始实施该技术,目标是为了向遗传性肿瘤的源头防控迈进。
该技术推出后,打破了以往仅针对单一基因的干预限制。它将研究视野扩展到多基因层面,以更全面的方式应对胚胎可能面临的癌症遗传风险,显现出显著的科研意义。
适用于亚洲人群的评估模型
考虑到亚洲女性乳腺癌的独特表现,新增了313份亚洲乳腺癌病例资料,并据此对现有的乳腺癌综合风险评估模型进行了优化。此次调整整合了乳腺癌易感基因变异和家族病史等风险因素,构建了一个更符合亚洲人群的乳腺癌风险评估体系。截至目前,该模型已有效识别出低风险胚胎。
结合本土人群特点构建模型,使得疾病风险评估更加精准与高效,这一举措完美契合了实际需求,并在医学界实现了重大进展。
多基因风险评分的现实意义
风险评估模型在预测子女遗传疾病风险上效果显著,其普遍应用对提升新生儿健康水平大有裨益。特别是针对家族有遗传病史(例如家族内有多名恶性肿瘤患者)且计划生育的适龄人群,这一评估显得尤为关键。家族内肿瘤患者数量较多时,更推荐在生育前进行风险评估。这一举措对于维护家族健康和后代福祉至关重要。
公众如何看待这一技术在家庭生育决策中的核心地位?我们热切期待大家踊跃发表意见、给予点赞并广泛分享。
